Jak zbudowany jest atom? W uproszczonym modelu atomu możemy wyróżnić małe lecz masywne jądro, naładowane ładunkiem dodanim oraz krążące wokół niego elektrony (jeden lub więcej) naładowane ładunkiem ujemnym.
1. Jądro atomu
Jądro atomu zawiera protony, naładowane ładunkiem dodanim i neutralne neutrony. Atomy tego samego pierwiastka zwierają taką samą liczbę protonów – nazywaną liczą atomową.
2. Powłoki elektronowe
Elektrony w atomie są przyciągane przez protony w jądrze. Ich uwolnienie wymaga dostarczenia elektronom energii z zewnątrz.
Elektrony o podobnym poziomie energii, krążą wokół jądra po zbliżonych orbitalach poruszając się w obrębie powłok elektronowych.
Ostatnią powłokę nazywamy powłoką walencyjną, a znajdujące się na niej elektrony – walencyjnymi. Liczba elektronów walencyjnych determinuje właściwości przewodnictwa elektrycznego ciał. Jeżeli powłoka walencyjna nie jest zapełniona to atomy podczas oddziaływania z innymi atomami uzupełniają lub opróżniają powłokę walencyjną.
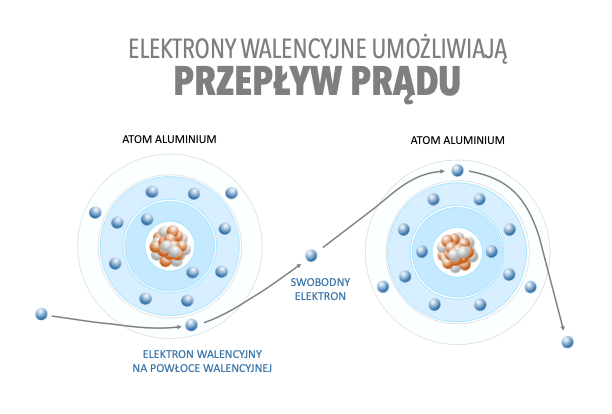
Przykład
Na powłoce walencyjnej aluminium znajduje się jedynie 3 elektrony a zmieścić może się na niej przynajmniej dodatkowe 5. To powoduje, że aluminium podobnie jak inne metale może łatwo uzupełnić lub opróżnić swoją powłokę walencyjną i w efekcie jest dobrym przewodnikiem prądu.
3. Ładunek atomu i jony
Atom o tej samej liczbie protonów i elektronów jest elektrycznie obojętny (nie przyciąga i nie odpycha). Atom, który stracił lub zyskał elektrony nazywamy jonem. Jony posiadają ładunek elektryczny.
- Atomy o większej liczbie protonów niż elektronów nazywamy jonami dodatnimi.
- Atomy o większej liczbie elektronów niż protonów nazywamy jonami ujemnymi.
PRZYDATNY ARTYKUŁ? Udostępnij link innym:

Następny temat:
Przewodniki i izolatory
Pozostałe tematy z działu: ELEKTROSTATYKA
Elektryzowanie ciał | Ładunek elektryczny | Jednostka ładunku elektrycznego: kulomb | Budowa atomu | Przewodniki i izolatory | Indukcja elektrostatyczna | Elektroskop | Prawo Coulomba

