W tym artykule znajdziesz najważniejsze informacje o pierwszej zasadzie termodynamiki: jej definicję, wzór na pierwszą zasadę termodynamiki oraz przykłady i zadania.
Pocierając o siebie zgrabiałe ręce lub zbliżając je do grzejnika lub ogniska – rozgrzewamy je, wykonując pracę lub absorbując ciepło. Pierwsza zasada termodynamiki to jedno z podstawowych praw termodynamiki, które głosi, że energię wewnętrzną ciała można zmienić jedynie dzięki oddziaływaniu z otoczeniem – przez wykonanie pracy lub przekazanie ciepła.
1. Definicja
Definicja pierwszej zasady termodynamiki: Energię wewnętrzną możemy zmienić przez wykonanie nad ciałem pracy lub przekazanie ciepła.
Co wynika z pierwszej zasady dynamiki?
- W układzie zamkniętym energia “nie ginie” i nie powstaje, może tylko zmieniać się z jednej postaci w drugą (pierwsza zasada termodynamiki jest sformułowaniem zasady zachowania energii)
- Nie jest możliwe zbudowanie maszyny, która mogłaby pracować ciągle bez pobierania energii z zewnątrz (tzw. perpetuum mobile)
- Praca i ciepło (cieplny przepływ energii) są równoważnymi sposobami przekazywania energii i są wyrażane w tych samych jednostkach (1 dżul). Uwaga: układ sam nie posiada pracy i ciepła – to sposoby przekazywanie energii
- Energia układu zamkniętego, który nie wymienia ciepła i nie wykonuje pracy (ani nie jest nad nim wykonywana praca) nie zmienia się
2. Wzór
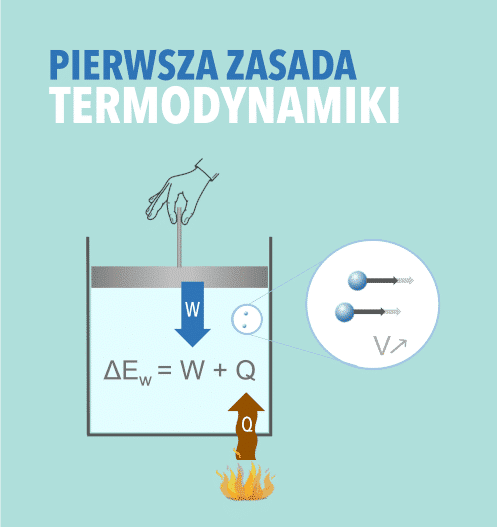
Pierwszą zasadę termodynamiki możemy zapisać wzorem: ΔEw = W + Q. Zmiana energii wewnętrznej ciała ΔEw jest równa sumie pracy W wykonanej nad tym ciałem oraz dostarczonego mu ciepła Q.
ΔEw = W + Q
ΔEw – zmiana energii wewnętrznej
W – praca wykonana nad ciałem
Q – ciepło dostarczone do ciała (cieplny przepływ energii)
Jednostką pracy i energii w układzie SI jest 1 dżul [J].
UWAGA: niekiedy możemy napotkać alternatywną wersję wzoru na zmianę energii wewnętrznej ΔEw = Q – W. W tym wypadku W oznacza prace wykonaną przez ciało (a nie nad ciałem) i dlatego posiada znak ujemny.
Zadanie:
Żelazko podczas prasowania dostarczyło tkaninie energii 10 J w wyniku tarcia oraz rozgrzało tkaninę energią 300 J. Jak zmieniła się energia wewnętrzna tkaniny?
Rozwiązanie:
W = 10 J
Q = 300 J
ΔEw = ?
ΔEw = W + Q
ΔEw = 10 J + 300 J = 310 J
Zauważmy, że jest to wartość dodania a więc energia wewnętrzna wzrosła.
Odpowiedź: Energia wewnętrzna tkaniny wzrosła o 310 J.
Rozszerzony wzór na pierwszą zasadę termodynamiki uwzględniający energię kinetyczną i potencjalna ciała to: ΔEp + ΔEk + ΔEw = W + Q.
3. Przykłady
Przykłady pierwszej zasady termodynamiki:
- Pocierając o siebie ręce w zimny dzień wykonujemy pracę przez co zwiększamy ich energię wewnętrzną i temperaturę
- Podgrzewając zupę dostarczamy jej ciepło co zwiększa jej energię wewnętrzną i temperaturę
- Dodanie kostek lodu do napoju spowoduje przepływ ciepła z napoju do kostek (ciepło zawsze przepływa z cieplejszego ciała do zimniejszego) zmniejszając energię wewnętrzną oryginalnej części napoju i jego temperaturę (uwaga: kostki “powiększą” ilość cząsteczek napoju a energia wewnętrzna zależy nie tylko od temperatury ale także od ilości cząsteczek)
- Pompując szybko oponę za pomocą pompki do roweru (wykonując pracę) możemy zaobserwować, że pompka się nagrzewa – jej energia wewnętrzna rośnie
- Lodówki, klimatyzatory oraz pompy cieplne zamieniają energię mechaniczną na ciepło wykorzystując fakt, że sprężanie gazu (przez wykonanie pracy) powoduje wzrost jego temperatury (i energii wewnętrznej) a rozprężanie spadek temperatury.
Zadanie:
W których sytuacjach opisanych poniżej energia wewnętrzna zmieniła się w wyniku przypływu ciepła a w których w wyniku wykonania pracy:
- Deska rozgrzała się podczas pocierania jej papierem ściernym
- Kowal rozgrzał metalowy element uderzając w niego młotem
- Zdejmując sweter poczuliśmy ciepło na plecach
- Podchodząc do kaloryfera poczuliśmy ciepło
- Pompując oponę rozgrzewamy pompkę
Rozwiązanie: W sytuacjach 1, 2, 5 energia wewnętrzna zmieniła się w wyniku wykonania pracy. W sytuacjach 3, 4 energia wewnętrzna zmieniła się w wyniku przepływu ciepła.
PRZYDATNY ARTYKUŁ? Udostępnij link innym:

Następny temat:
Przewodnictwo cieplne
Pozostałe tematy z działu: TERMODYNAMIKA
Temperatura | Skale temperatur | Energia wewnętrzna | Przepływ energii (ciepło) | Jednostka ciepła: dżul | Pierwsza zasada termodynamiki | Przewodnictwo cieplne | Zjawisko konwekcji | Ciepło właściwe | Zmiany stanów skupienia | Topnienie i krzepnięcie | Parowanie i skraplanie

